Европейская комиссия предложила отложить вступление в силу новых требований к безопасности медицинских устройств на 2027—2028 годы, в зависимости от класса риска. Таким образом регулятор надеется избежать дефектуры медицинских изделий.
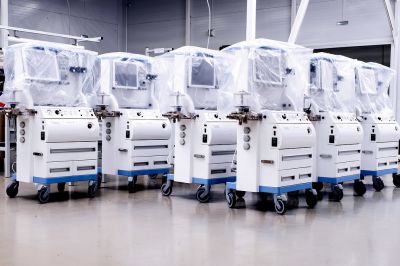
Европейская комиссия внесла в Европейский парламент предложение продлить переходный период для введения Регламента о медицинских устройствах (Medical Devices Regulation) для устройств с более высоким уровнем риска до конца 2027 года, а для устройств со средним и низким уровнями риска — до конца 2028 года. Ранее производители предупредили комиссию, что им проще прекратить производство некоторых устройств, чем выполнить новые требования, пишет MedTechDive.
«Сейчас крайне важно, чтобы Европейский парламент и Совет приняли это законодательное предложение как можно скорее, чтобы восстановить приемлемый путь регулирования, который позволит всем категориям медицинских устройств оставаться доступными для пациентов и систем здравоохранения», — говорится в заявлении Ассоциации производителей медицинских устройств MedTech Europe.
В соответствии с Medical Devices Regulation, вступившим в силу в мае 2021 года, все медицинские устройства, от имплантатов и протезов до глюкометров и катетеров, должны соответствовать более строгим критериям безопасности. Иногда это предполагает проведение новых клинических испытаний, что для производителей оборачивается большими временными и финансовыми затратами.
Принятие Medical Devices Regulation уже несколько раз откладывалось (на эти правила должны были перейти еще в 2020 году по окончании трехлетнего переходного периода), потому что производители предупреждали, что это положит конец инновациям и приведет к дефектуре некоторых устройств.
 Химки ИНФО – ещё ближе к городу Новости Химок, важные события и происшествия, инфопортал Химки ИНФО – самые свежие и популярные новости.
Химки ИНФО – ещё ближе к городу Новости Химок, важные события и происшествия, инфопортал Химки ИНФО – самые свежие и популярные новости.